2. Eter
Eter merupakan isomer fungsi dari alkohol. Eter memiliki rumus umum R – O – R, dengan R adalah alkil. Alkil-alkil pada eter dapat disamakan dan dapat pula dibedakan.
Ada dua cara pemberian nama eter, yaitu nama IUPAC dan nama lazim.
Nama IUPAC
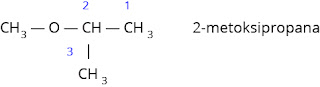
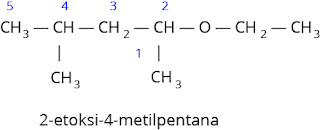
Nama IUPAC eter adalah alkoksi alkana. Eter dianggap sebagai turunan alkana yang satu atom H diganti oleh gugus alkoksi (–OR).
Jika gugus alkilnya berbeda, alkil yang dianggap sebagai alkoksi adalah alkil yang rantai C-nya lebih pendek, sedangkan alkil yang rantainya lebih panjang dianggap sebagai alkana (rantai pokok).
Penomoran dimulai dari C ujung yang terdekat dengan posisi gugus fungsi sehingga C yang mengandung gugus fungsi mendapat nomor terkecil.
Contoh:
Nama trivial
Eter diberi nama alkil-alkil yang mengapit – O – menurut abjad dan diikuti dengan kata eter.
Contoh:
CH3-O-CH2-CH3 etil metileter
CH3-CH2-O-CH2-CH2 dietileter
b. Isomer fungsi antara eter dan alkohol
Alkohol dan eter mempunyai rumus molekul sama tetapi gugus fungsinya berbeda. Oleh karena itu, alkohol dan eter disebut sebagai berisomer fungsi.
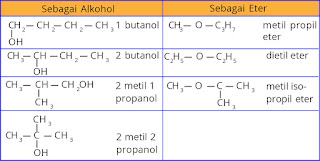
Di bawah contoh rumus molekul beberapa alkohol dan eter.
Isomer dari C4H10O dapat berupa alkohol maupun eter.
Sifat fisis
Suhu-suhu eter yang rendah mudah menguap dan mudah terbakar. Titik didihnya rendah karena tidak mempunyai ikatan hidrogen. Sukar larut dalam air.
1) Berupa zat cair (kecuali metil eter) berbau harum dan mudah menguap.
2) Dengan jumlah atom C yang sama, titik didih eter lebih rendah dari titik didih alkohol.
3) Sukar larut dalam air.
Sifat kimia
1) Tidak bereaksi dengan logam Na dan PCl3, dengan demikian dapat untuk membedakan alkohol dengan eter.
2) Bereaksi dengan PCl5, tetapi tidak membebaskan HCl (reaksi ini dapat digunakan untuk membedakan alkohol dengan eter).
4) Dengan HI berlebih dan pemanasan menghasilkan R – I dan H2O.
5) Eter mudah terbakar membentuk gas CO2 dan uap air.
d. Pembuatan Eter
Dengan eliminasi alkohol pada suhu 140°C.
e. Kegunaan eter
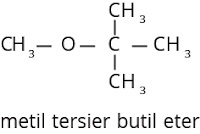
Dalam kehidupan sehari-hari eter yang paling banyak digunakan adalah dietil eter, yaitu sebagai obat bius dan pelarut senyawa nonpolar. MTBE (metil tersier butil eter) ditambahkan ke dalam bensin untuk meningkatkan bilangan oktan.




EmoticonEmoticon